商品名称:LuciFida
生产商:卢修斯制药 Lucius
中文名称:非达霉素
英文名称: Fidaxomicin
【概括】
适用于成人和儿童患者的艰难梭菌相关腹泻(CDAD)的治疗。
【适应症】
1、艰难梭菌相关性腹泻
非达霉素适用于6个月及以上的成人和儿童患者,用于治疗艰难梭菌相关性腹泻(CDAD)。
2、使用
为了减少耐药菌的产生并保持非达霉素和其他抗菌药物的有效性,非达霉素应仅用于治疗经证明或强烈怀疑由艰难梭菌引起的感染。如果有培养物和敏感性信息,则在选择或修改抗菌治疗时应考虑这些信息。在缺乏此类数据的情况下,局部流行病学和易感性模式可能有助于经验性选择治疗。
【规格】 200mg/片,20片/瓶
【用法用量】
1、重要管理说明
非达霉素可制成200毫克片剂口服给药,也可制成颗粒剂口服混悬剂(40毫克/毫升 (200毫克/5毫升)(当重新配制时))。非达霉素可与食物一起或单独口服。
2、成年患者
成人的推荐剂量为每日两次口服一片200毫克非达霉素片剂,持续10天。
3、儿童患者(6个月至18岁以下)
1)片剂
体重至少12.5千克且能吞咽片剂的儿童患者的推荐剂量为每日两次口服一片200毫克非达霉素片剂,持续10天。如果无法吞咽片剂,可按照下表中的建议向儿童患者给予非达霉素口服混悬液。
2)口服混悬液
基于体重的儿科患者推荐剂量见下表。使用口服给药注射器口服非达霉素口服混悬液,每日两次,持续10天。
表:非达霉素口服混悬液在儿童患者中的推荐剂量(基于体重)
非达霉素口服混悬液在儿童患者中的推荐剂量(基于体重)
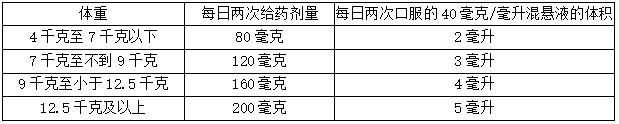
4、非达霉素口服混悬液的制备及给药
1)准备
a.摇晃玻璃瓶,确保颗粒自由移动,没有结块。
b.取130毫升纯化水,加入玻璃瓶中,并盖上盖子。
c.将瓶子保持在水平位置,并在该位置用力摇晃瓶子至少2分钟。
d.验证是否获得了均匀的悬浮液。如果没有,重复摇晃步骤。
e.目视确认悬浮液均匀后,再摇晃30秒。
f.将瓶子静置1分钟。
g.验证悬浮液是否仍然均匀。如果没有,请重复步骤a至f。
h.一旦重新配制,非达霉素口服混悬液的颜色为白色至黄白色。
i.在瓶子上写下报废日期(当前日期加上12天)。
2)复原口服混悬液的储存
将重构的口服混悬液储存在冰箱2°C-8°C中最长12天。12天后丢弃。
3)管理
1.每次给药前15分钟从冰箱中取出药瓶。
2.用力摇晃,直至悬浮液具有均匀的稠度。
3.取下盖子,然后使用口服给药注射器在有或无食物的情况下进行口服给药。
4.在两次给药之间,更换盖子并储存在冰箱中。
【 不良反应】
1、临床试验体会
由于临床试验在各种各样的条件下进行,因此无法将一种药物临床试验中观察到的不良反应发生率与另一种药物临床试验中的发生率直接进行比较,并且可能无法反映实际中观察到的发生率。
1)成年人
在两项主动对照试验中,对564例CDAD病成人患者进行了非达霉素200毫克片剂的安全性评估,其中86.7%的患者接受了完整疗程的治疗。
33名接受非达霉素治疗的成人患者(5.9%)因不良反应(AR)退出试验。导致退出研究的AR类型差异很大。呕吐是导致停用给药的主要不良反应;在3期试验的非达霉素和万古霉素患者中,这种情况的发生率均为0.5%。下表列出了在≥2%接受非达霉素治疗的成人患者中发生的最常见选定不良反应。
表:对照试验中接受非达霉素治疗的成人患者报告的发生率≥2%的选定不良反应
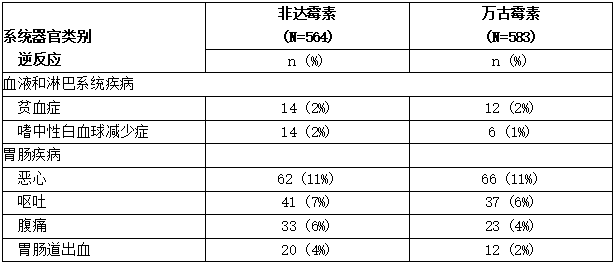
对照试验中接受非达霉素治疗的成人患者报告的发生率≥2%的选定不良反应
在对照试验中,在< 2%服用非达霉素片剂的成人患者中报告了以下不良反应:
胃肠疾病:腹胀、腹部压痛、消化不良、吞咽困难、肠胃气胀、肠梗阻、巨结肠
免疫疾病:血液碱性磷酸酶升高,血液碳酸氢盐减少,肝酶增加,血小板计数减少
代谢和营养障碍:高血糖、代谢性酸中毒
皮肤和皮下组织疾病:药疹、瘙痒、皮疹
2)儿科
在对38名患者进行的2期单臂试验以及对98名接受非达霉素治疗的患者和44名接受万古霉素治疗的患者进行的3期随机、活性对照试验中,评估了非达霉素在6个月至18岁以下儿童患者中的安全性。在两项研究中,患者均口服非达霉素每日两次,持续10天。年龄< 2岁、或体重< 12.5千克、或无法吞咽片剂的患者接受了基于体重的非达霉素口服混悬液给药。体重至少12.5千克且能吞咽片剂的患者服用了200毫克非达霉素片剂。2期试验的年龄范围为11个月至17岁,3期试验的年龄范围为1个月至17岁(1例患者年龄小于6个月)。
在2期单臂试验中,有1例死亡病例。在3期试验中,非达霉素治疗的患者在研究期间(40天)有3例死亡,万古霉素治疗的患者没有死亡。所有死亡病例均发生在 2 岁以下的患者身上,似乎与潜在的合并症有关。
在2期试验中,有7.9%(3/38)的患者因不良反应而中断治疗;在3期试验中,非达霉素和万古霉素治疗的患者中分别有1%(1/98)和2.3%(1/44)的患者因不良反应而中断治疗。下表列出了在第3期试验中接受非达霉素治疗的儿童患者中发生率≥5% 的最常见选定不良反应。
表:对照试验中接受非达霉素治疗的儿童患者报告的发生率≥5%的选定不良反应
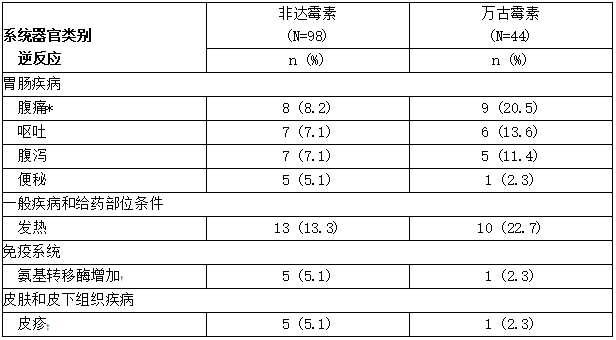
* 包括腹痛、下腹痛和上腹痛
† 包括丙氨酸转氨酶升高、天冬氨酸转氨酶升高和肝酶升高
‡ 包括皮疹、滤泡性皮疹、斑丘疹和剥脱性皮疹
临床试验中< 5%服用非达霉素的儿童患者报告了以下不良反应:皮肤和皮下组织疾病:荨麻疹、瘙痒
2、上市后体验
在批准后使用非达霉素期间发现了以下不良反应。由于这些反应是从规模不确定的人群中主动报告的,因此并不总是能够可靠地估计其频率或确定与药物暴露的因果关系。
过敏反应(呼吸困难、血管性水肿、皮疹、瘙痒)
【 注意事项】
1、过敏反应
非达霉素曾报告过急性过敏反应,包括呼吸困难、皮疹、瘙痒以及口、喉和面部的血管性水肿。如果出现严重的过敏反应,应停用非达霉素并开始适当的治疗。
对非达霉素有过敏反应的部分患者还报告有对其他大环内酯类药物过敏史。对已知大环内酯类药物过敏的患者开非达霉素处方的医生应意识到过敏反应的可能性。
2、不适用于艰难梭菌相关腹泻以外的感染
由于非达霉素的最小系统吸收,预计非达霉素对治疗其他类型的感染无效。除CDAD外,尚未对非达霉素进行其他感染治疗研究。非达霉素应仅用于治疗CDAD病。
3、耐药菌的研究进展
在没有经证实或强烈怀疑艰难梭菌感染的情况下开非达霉素处方不太可能为患者带来益处,并且会增加耐药性细菌产生的风险。
【特殊人群用药】
1、妊娠期
关于孕妇使用非达霉素的可用数据有限,不足以告知重大出生缺陷、流产或不良母体或胎儿结局的任何药物相关风险。在器官发生期间静脉注射的动物中进行的胚胎-胎仔生殖研究显示,在fidaxomicin和OP-1118(其主要代谢产物)暴露量是非达霉素推荐剂量临床暴露量的65倍或更高时,没有证据表明对胎儿有伤害。
2、哺乳期
没有关于人乳汁中存在fidaxomicin或其主要代谢产物OP-1118、对母乳喂养婴儿的影响或对产奶量的影响的信息。在考虑母乳喂养对发育和健康的益处时,应同时考虑母亲对非达霉素的临床需求以及非达霉素或潜在母体疾病对母乳喂养婴儿的任何潜在不良影响。
3、儿童使用
非达霉素治疗CDAD病的安全性和有效性已在6个月至18岁以下的儿童患者中得到证实。在这些年龄组中使用非达霉素有证据支持,这些证据来自非达霉素在成年CDAD患者中进行的充分且对照良好的试验,以及来自儿科试验的药代动力学、安全性和疗效数据。在儿科试验中,未发现与在儿科患者中使用非达霉素相关的新的安全性信号。
尚未确定非达霉素在6个月以下儿童患者中的安全性和有效性。
4、老年用药
在非达霉素对照试验的患者总数中,50%为65岁及以上,31%为75岁及以上。与万古霉素相比,在这些受试者和较年轻的受试者之间未观察到非达霉素的安全性或有效性的总体差异。
在对照试验中,与非老年(
【禁忌症】
在已知对非达霉素或非达霉素中的任何其他成分过敏的患者中禁用。
【药物相互作用】
非达霉素及其主要代谢物 OP-1118 是胃肠道中表达的外排转运体 P 糖蛋白(P-gp)的底物。
1、环孢霉素
环孢霉素是包括P-gp在内的多种转运体的抑制剂。当环孢霉素与非达霉素联合给药时,fidaxomicin和OP-1118的血浆浓度显著升高,但仍保持在ng/mL范围内。在作用部位(即胃肠道),也可能通过P-gp抑制作用降低菲达霉素和OP-1118的浓度;然而,在对照临床试验中,合用P-gp抑制剂对接受氟达霉素治疗的成人患者的安全性或治疗结果没有可归因的影响。基于这些结果,可以将菲达霉素与P-gp抑制剂联合给药,不建议调整剂量。
【药物过量】
未报告人类急性用药过量病例。在犬中以9600毫克/天(超过人剂量的100倍,按重量比)剂量服用fidaxomicin片剂3个月,未观察到与药物相关的不良作用。
【成分】
有效成分:fidaxomicin
片剂: 薄膜包衣片,每片含200毫克的fidaxomicin和以下非活性成分:丁基化羟基甲苯、羟丙基纤维素、卵磷脂(大豆)、硬脂酸镁、微晶纤维素、聚乙二醇、聚乙烯醇、预胶化淀粉、淀粉羟乙酸钠、滑石粉和二氧化钛。
【性状】片剂
【贮存方法】
非达霉素片剂
储存温度为 20°C-25°C;允许偏离至 15°C-30°C 。参见 USP 控制室温。储存在原瓶中。

老挝国家药品批准文号:04 L 1089/24
厂家信息:
药企介绍
卢修斯制药(老挝)有限公司(简称卢修斯制药),是一家现代跨国高新生物制药企业。目前拥有1个全球研发中心,与3家业内顶尖的研发团队合作,擅长复杂化学制剂及生物制剂研发,实现了关键仿制药品技术突破,目前卢修斯制药已成为全球专利仿制药研发能力最强的企业之一,在业界拥有良好的声誉的和市场口碑。
2020年卢修斯制药正式开启亚太战略,斥巨资在老挝首都万象投建亚太1号智慧工厂,按照GMP生产标准,引进中国、美国、德国等世界尖端制药设备,成立国际化高端制剂车间,年仿制药生产能力超15亿片。产品现已涵盖抗肿瘤、心血管、血液,糖尿病、皮肤病、男性保健、抗衰老等200多种品类,远销欧洲、南美洲、非洲、中东、印度、越南、尼泊尔等50多个国家和地区。
卢修斯在老挝建设了目前老挝最高标准的药品生产车间,自从老挝卢修斯建厂投产后, 公司将协同东南亚国家联盟,加快国际化进程,加强全球医药研发智力合作,丰富产品、提升质量,努力成为全球领先制药企业。
卢修斯制药的生产环境完全符合老挝、欧盟、美国和中国等国家的GMP(Good Manufacturing Practice,良好生产规范)标准。这意味着卢修斯制药的生产过程严格遵守了全球公认的质量管理和质量控制标准。

老挝卢修斯制药GMP认证证书
老挝卢修斯制药通过其先进的设施、严格的质量控制和广泛的业务范围,已经成为了老挝制药行业的一个重要玩家。
有了生产设备和车间,那么生产的药品质量怎么样呢?
老挝卢修斯的生产的每款药品都经过严格的检测,可以肯定的是老挝卢修斯仿制的药物药效是达到标准的,是完全放心的产品,
卢修斯的产品都是经过严格实验和检测,确保了产品的可靠,放弃购买老挝卢修斯制药的产品,可能就真的失去了一款药效可靠且还能省钱的机会。因为服用过老挝卢修斯产品的患者发现,服用价格低廉的卢修斯药品和之前服用其他药厂较高较高的产品药效竟然是完全一致。

世界卫生组织对老挝卢修斯进行访问并进行肯定

老挝卢修斯参加迪拜国际医药会展
卢修斯制药作为全球卫生健康守护者,尖端制药行业精进者,秉承“关爱生命、服务健康”这一理念,与各国共同致力于提高优质医疗知识资源的生产、共享和利用,努力增强和维持肿瘤、艾滋病和免疫系统等疾病的预防治疗和护理,尤其发挥公司全球抗癌制药关键技术优势和抗癌产品质优价廉的特点,防范和降低危害人类健康。







 匿名用户
匿名用户  匿名用户
匿名用户